麗寶新藥(代號 7888)是以介白素 IL-12 做免疫調節細胞激素為核心技術的新藥開發公司。麗寶新藥透過調整劑型的穩定特性/安全性高,與緩釋(slow relase)效果,來達成控制血液腫瘤等罕見疾病等適應症。麗寶新藥除了在造血相關的急性輻射症候群(HSARS)的新藥開發之外,就以 CTCL(皮膚T細胞淋巴瘤)與 DBTCL(瀰漫性大B細胞淋巴瘤)等相關適應症為優先開發。法人指出,因為 CTCL 等算是罕見疾病,以介白素技術所研發之中新藥,再加上化療與放療等合併療法及其他免疫治療為主;若加計其他“合併療法”初算約 100 億美元產值;其中,麗寶新藥專注的 CTCL 病症的目標群體是以歐美市場為主、尤以是白人男性為大宗,全球市場產值約 10 億美元。麗寶新藥現今競爭優勢,可從 CTCL 的二期臨床 Phase 2a 受試者治療 8 個月之後的整體反應率為 64%(指合併治療組/即化療 or 放療,再加上 LIB-101 研發中的新藥)看得出來,優於傳統療法 LD-TSEBT(全身性皮膚電子束照射)的對照組的 21% 的反應療效。公司將於 2026 年下半年與 FDA 討論三期臨床試驗的設計,若順利的話,將於 2H26 推進到 CTCL 的 3 期臨床試驗。
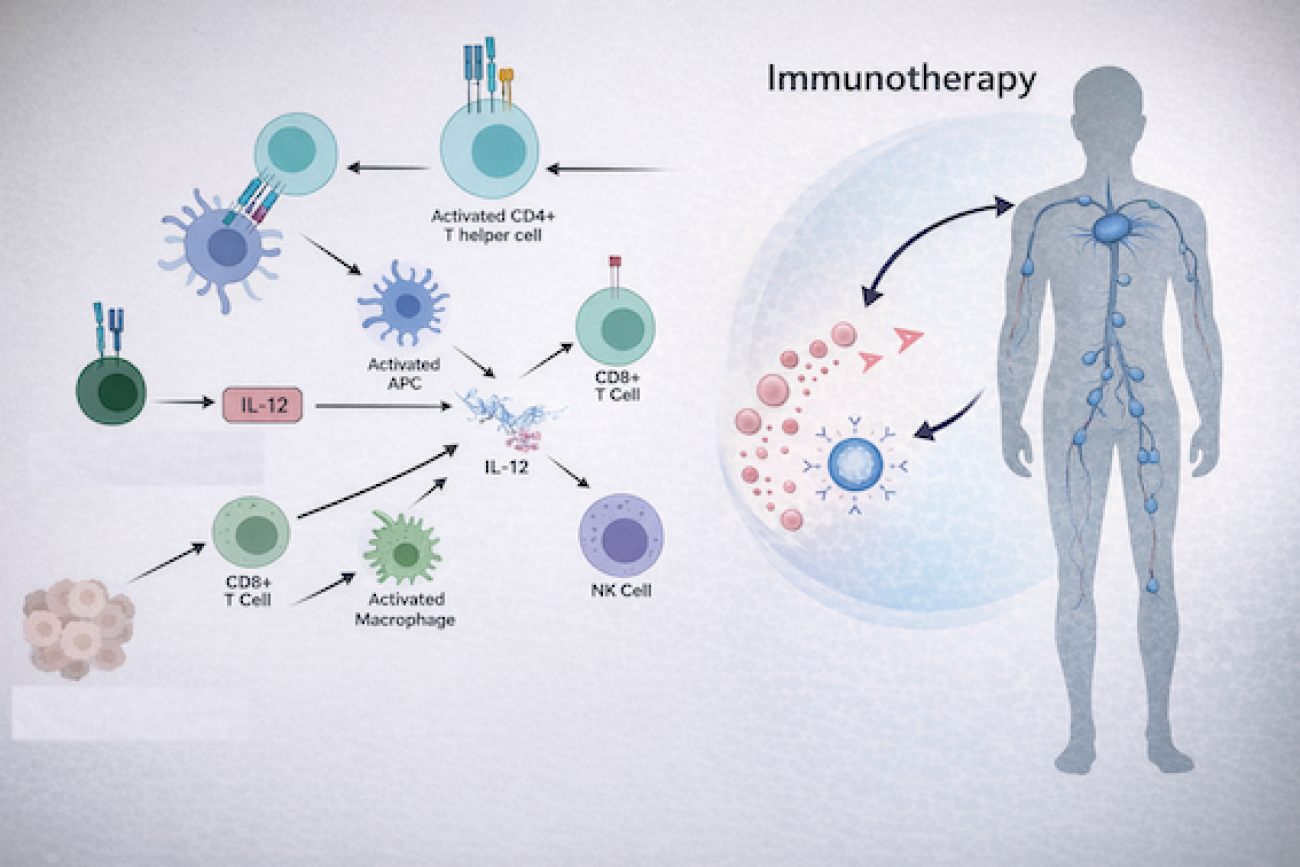
(麗寶 LIB-101/IL-12 介白素免疫風暴低,淋巴瘤優先)
麗寶新藥先以國防(急性輻射)醫療 + 免疫療法雙主軸的新藥開發策略:
經營團隊在回覆如何維持目前的雙主軸成長時?麗寶新藥總經理暨創辦人劉朝瀚表示,國防醫療與免疫療法各具特色。國際情勢與核能的新技術開展,因此 HSARS(緊急輻射症候群)潛在需算廣大,受眾途徑主要採購是政府單位或核電廠、甚至私人單位,銷售管道比較明確,是公司成穩定發展基石,創造穩定現金流。在免疫藥物免疫療法持續發展,外界將更期待皮膚T細胞淋巴瘤(CTCL;Cutaneous T-Cell Lymphoma)與瀰漫性大B細胞淋巴瘤(DLBCL;Diffuse Large B-Cell Lymphoma)的更大商機。
麗寶新藥在淋巴瘤等罕見適應症,以全球銷售授權為主:
在加速國際市場能見度及跨國合作上,麗寶新藥表示,藥物開發有跟國際不同醫療單位、KOL(藥物開發業界意見領袖)及政府單位有不同程度合作;經過長期合作關係奠定雙方互信。在藥物開發階段,合作對象能瞭解公司產品特性及競爭優勢,有助於公司將來商業擴展以及市場開發。
麗寶新藥 2025 年 7 月已完成 8.5 億元台幣現金增資,支持公司 2026 年目前的規劃及項目推進。麗寶新藥指出,將定期檢視資金使用狀況與執行,亦不排除接下來可能會新項目或合作計畫、將其評估與報告提報董事會。對於是否會有下一步募資的想法則留於內文中討論。
麗寶新藥第一個外部股東、在 2018 年投資的台安生技曾經建議公司是否再投入更多 CMC(化學生產控制;Chemistry Manufacure Control)來協助其他國內生技公司,這部份日後投資人們可觀察公司營運上是否納入更多策略。
本篇全篇文章〔麗寶新藥 2026 年興櫃登錄之後 問答〕有 1 字頭高位數的討論,分為臨床試驗與開發相關(LIB-101 臨床布局與 CTCL 上的想法)、財務與營運相關(短期營運重點與資金應用)、病症相關(怎麼看淋巴瘤等血液腫瘤)、介白素開發與同業競爭相關(國際同業與公司在不同介白素(Interleukin)的重點)等四大面向。
※ 全文文章內容 = 聚焦文章內容 + 增補文章內容。已購買標題結尾有(全)字之全文文章,無需再買聚焦文章、增補文章(標題結尾有(增)字),因為內容都一致。全文章、聚焦文章有含【Key Points】;另,僅全文章、增補文章有財務報表。新加入會員,應先詳讀◎〔購物.更新 〕分頁◎說明;內容型態網站不可退費,已購買全文章、自行重覆購買聚焦文章、增補文章,無任何退費機制。
(一)麗寶發展沿革與基本資料:
- 公司成立於 2017 年迄今約九年;主要在精進技與製程最佳化。近年重點在轉換技術與在臨床上的發展。登錄興櫃時的資本額 7.52 億元,員工人數約 30 人。
- 主軸產品 LIB-101;用於適應症包括緊急輻射症候群(HSARS)、剛完成的二期臨床,即將邁向臨床三期。下個重點適應症是「皮膚T細胞淋巴瘤(CTCL)」、亦已完成 Phase 2a。
- CTCL 預計將進一步邁向 Phase 2b 與 3 期。
- 急性輻射症候群與淋巴瘤等適應症,皆取得孤兒藥資格。目前是國防醫療(指緊急輻射症候群)加上免疫藥物(指皮膚T細胞淋巴瘤/CTCL)雙主軸新藥開發公司。
- 最早創始資金是麗寶集團,加上外部投資人台安生技的支持,後續有 B 輪、C 輪等投資人加入各階段藥物開發資源或協助。
- 為了能在藥品上順利開發,同時也降低風險、有效資源整合,麗寶新藥採取三階段發展策略:
- ⑴ 第一階段的戰備防護,
- ⑵ 第二階段發展罕病腫瘤(指淋巴瘤),
- ⑶ 第三階段邁向到多重適應症(舉例,如大腸直腸癌、肺癌、與業界 CAR-T 的合作等實體腫瘤)的開發上。
- 【Remind】:其第一階段與第二階段,算是罕病的範疇(小眾市場)。而“長遠”第三階段,則算是大眾化的適應症市場。