國邑藥品科技(代碼 6875)登錄興櫃之初準備 3 項產品,現階段收窄至兩項,繼授權出去給 Liquidia 的 L606 後,下個重點是 L608。其適應症分別是 ① 系統性硬化症相關,還有 ② 第一類肺動脈高壓疾病 PAH。在 L608 的 PAH 開發上,2023 年已於澳洲進行臨床一期,等到該臨床能整合的共同藥動資料,就拿來做為雷諾氏症(SSc-RP)與指潰瘍(DU)的開發;SSc-RP/DU 擬於美國與歐洲討論臨床二/三期設計。
L608 在硬化症適應症作全球開發,在肺動脈高壓適應症主攻非北美(歐/中/台)市場:
國邑 L608 開發雷諾氏症(◎SSc-RP◎)與指潰瘍(◎DU◎)已取得美國罕病資格,但更放眼全球市場;後續也會在歐洲、中國洽談區域授權。
您或許會察覺,L608 與 L606 都有開發第一類肺動脈高壓病症 PAH。差別在於 L606 是北美市場,而 L608 是鎖定非北美市場。前一篇聚焦文章有製做表格,並於內文依藥理來說明。
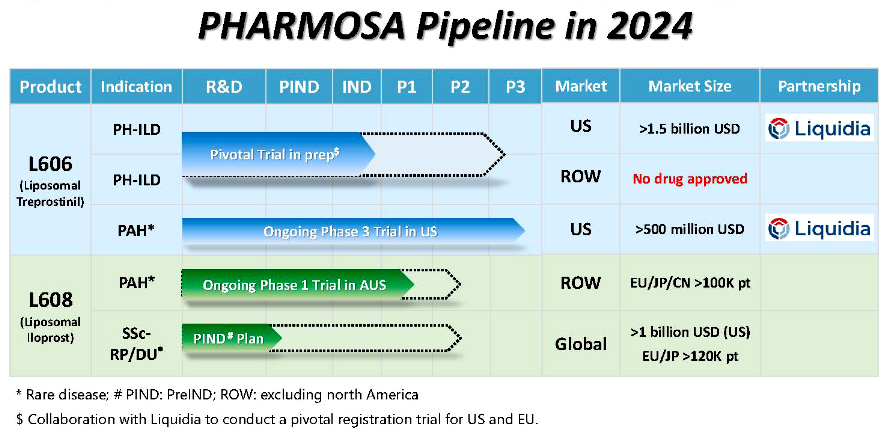
國邑 L606 與 L608 產品在 2024 年的進展 pipeline (來源:國邑法說會簡報)
國邑總經理甘霈認為,日本、歐洲、中國、台灣在罕病 PAH 主要一線用藥,還是 Ventavis ,其用藥流程常且頻繁,對病人非常不友善。雖然,日本 2023 年也對 PAH 病友核准了藥物 Tyvaso ,剩下的歐洲、中國、台灣等地仍需要開發服藥更方便產品。
國邑授權+IPO後資金充裕,費用支出亦心理有譜;除續推動 L608 一期,規劃安瓿充填產能也是重點:
國邑 L608 用於 PAH 的全球(北美以外)取證會以 Ventavis 為對照藥物,經由 Hybrid 或新藥 2.2 法規申請,各區域可討論減免試驗要求(像是,一期後直接進入三期),預計可快速滲透目標市場。
本篇增補文章也針對國邑的遞送藥物技術「微脂體(Liposome)」平台,短期內“營業費用”方向與資金需求想法,以及接下來的安瓿充填線產能配置與布局作問答式說明;以及公司為何會挑選了 Liqudia 藥廠作為夥伴原因。而也從公司的澳洲臨床一期與藥動取得的時間,衡量出 2025 年澳洲臨床應可以進入臨床二/三期。
- ☆本篇為聚焦文章《國邑夥伴L606臨床3期,助歐/日/中 PH-ILD 授權 2024 Feb》增補文章。若您曾購買了上述『聚焦文章』,請您回到該聚焦文章末尾【優惠價格連結】、以更實惠的加價購買此『增補文章』。
- ☆再次提醒您,「若您在此以『原價』購買此篇,視同放棄自『聚焦文章』加價購優惠價權益」;您一旦完成註冊成為會員程序,代表您已知悉所有付費文章,購買後皆無退費條款,本網站無法赴第三方交易平台為您作任何退費與協助重購,特此聲明。
國邑夥伴L606臨床3期,助歐/日/中 PH-ILD 授權 2024 Feb 國邑設充填線,L608擬 2025 澳洲二/三期臨床 2024 Feb(增)